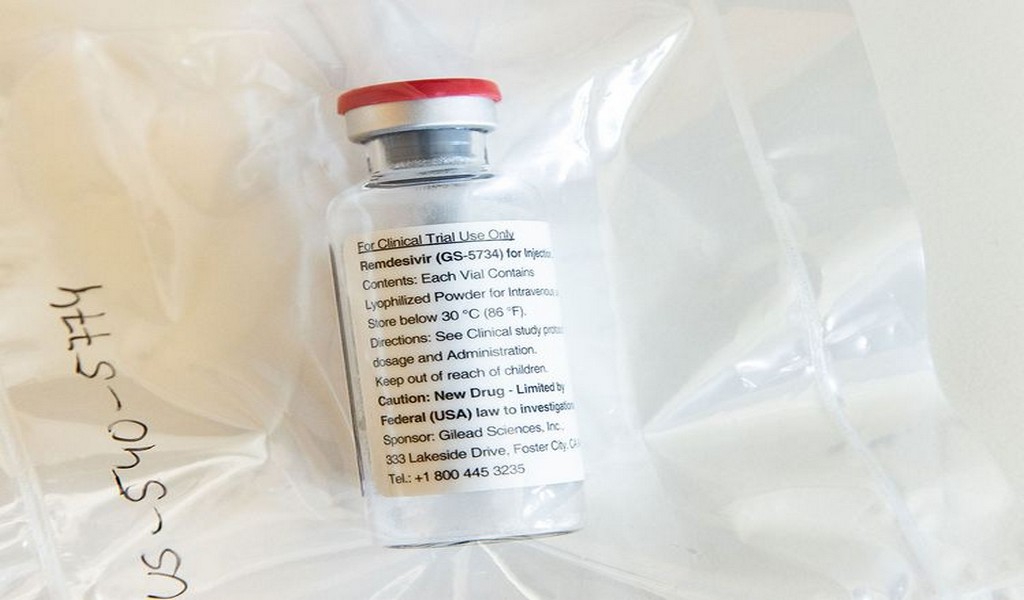
Dubai: Remdesivir todavía se considera un antiviral experimental, patentado en los Estados Unidos, con otra solicitud de patente en China. Su licencia estadounidense está bajo el caso de "uso de emergencia" en pacientes con coronavirus.
Desarrollado por la firma estadounidense de biotecnología Gilead Sciences, remdesivir se patentó por primera vez en 2017, cuando la compañía lo estaba buscando originalmente como un posible tratamiento para el virus del Ébola, que estalló por primera vez en 2013-14.
En los ensayos, se observó que remdesivir ayudaba a reducir las tasas de mortalidad hasta un 33% entre los pacientes con ébola, si las víctimas recibían el tratamiento lo suficientemente temprano después de enfermarse cuando las cargas virales todavía estaban ahora, según un informe de Wired en diciembre de 2019.
Sin embargo, se informó que al menos otros tres tratamientos contra el ébola funcionan mejor para reducir las muertes, en comparación con remdesivir después de ensayos en África. Estos son: ZMapp (por Mapp Biopharmaceutical Inc), mAb114 (por el Instituto Nacional de Alergias y Enfermedades Infecciosas de EE. UU., NIAID) y el REGN-EB3 de Regeneron, según el informe Wired .
Pero debido a las similitudes bioquímicas en la forma en que funcionan los virus Ébola y SARS-CoV-2, Gilead había visto la oportunidad de "reutilizar" remdesivir para tratar COVID-19 a principios de 2020.
Un estudio publicado en enero de 2020 en el New England Journal of Medicine informó que un paciente con coronavirus de EE . UU . Mostró una mejoría después de tomar remdesivir .
El ébola se infiltra en las células de sus víctimas a través de proteínas puntiagudas en la capa externa del virus. El virus mortal causa fiebre, dolores corporales y diarrea. En muchos casos, a medida que el virus se propaga, también provoca sangrado dentro y fuera del cuerpo, ya que destruye el sistema inmunitario y los órganos. En última instancia, hace que disminuyan los niveles de células que coagulan la sangre, lo que en última instancia puede ser fatal.
Sin embargo, el virus SARS-CoV-2 actúa de la misma manera utilizando una proteína de punta que se une fácilmente a ACE2 (enzima convertidora de angiotensina 2), la proteína receptora de SARS-CoV y SARS-CoV-2, que es abundantemente presentes células epiteliales de pulmón humano e intestino delgado. El virus golpea los pulmones.
¿Cuál es el precio justo para remdesivir?
En 2018, The Lancet publicó un estudio que estima el costo de desarrollar al menos una vacuna hasta el final de la fase 2a para cada una de las 11 enfermedades infecciosas epidémicas, con un mínimo de $ 2.8 mil millones a $ 3.7 mil millones (o entre $ 1.2 mil millones a $ 8.4 rango de mil millones).
El Instituto de Revisión Clínica y Económica (ICER), un equipo de investigación sin fines de lucro de Massachusetts que estudia los costos de desarrollo de medicamentos, dice que remdisivir es rentable a $ 4,460 por curso de tratamiento.
El Instituto de Revisión Clínica y Económica (ICER), una organización sin fines de lucro con sede en Boston que estudia los costos de los medicamentos, dice que el medicamento es rentable a $ 4,460 por curso de tratamiento.
Gilead, con sede en California, ahora está aumentando la oferta con el objetivo de tratar a 1 millón de pacientes para fin de año, según un informe .
Este mes, Beximco Pharmaceuticals, uno de los mayores fabricantes de medicamentos de Bangladesh , comenzará a remdesivir la producción bajo la licencia de Gilead, dijo un alto ejecutivo de la compañía.
Según un informe de Reuters del miércoles (5 de mayo de 2020), la compañía planea ponerle un precio al medicamento, administrado por infusión intravenosa, entre $ 59- $ 71 / por vial , según el director de operaciones de Beximco, Rabbur Reza, y agregó que un paciente podría necesitar en cualquier lugar entre 5 y 11 viales.
Las patentes remdesivir de Gilead significan que tiene el monopolio de la droga en los Estados Unidos. Salvo la acción del gobierno o Gilead autorizando la patente a otros, es la única compañía que puede fabricarla.
La patente de Gilead expira en 2037, momento en el que podría ser posible una versión genérica.
El 4 de febrero de 2020, Reuters informó que el Instituto de Virología de Wuhan (WIV) había solicitado una patente sobre el uso del remdesivir de Gilead en China
. La solicitud fue presentada conjuntamente con el Instituto de Medicina Militar de China de la Academia de Ciencias Militares del Ejército Popular de Liberación, según el Instituto de Virología de Wuhan.
Ese fue el mismo día en que Cell Research publicó los resultados de un estudio clínico en China que muestra que remdesivir y cloroquina, juntos, "inhibieron efectivamente" el SARS-CoV-2 (entonces llamado 2019-nCoV) in vitro.
Remdesivir y la investigación de células de cloroquina.
El estudio de reutilización de fármacos publicado en Cell Research el 4 de febrero de 2020. Establece: "Un enfoque eficiente para el descubrimiento de fármacos es probar si los fármacos antivirales existentes son efectivos en el tratamiento de infecciones virales relacionadas".
Crédito de imagen: Cell Research / Screengrab Una de las autoras de ese estudio fue la profesora Shi Zhengli, también conocida como la "mujer murciélago" china acreditada por su extensa investigación sobre coronavirus de murciélago, incluidos los estudios de WIV financiados por el gobierno de los Estados Unidos .
El 2 de mayo de 2020, las autoridades de los EE. UU. Aprobaron remdesivir para uso de emergencia en pacientes con coronavirus, a medida que más estados de EE. UU. Redujeron los bloqueos a pesar de otro aumento en las muertes por la enfermedad.
La aprobación de los Estados Unidos es el último paso en un esfuerzo global para encontrar tratamientos viables y una vacuna para el coronavirus, que infectó a más de 3,3 millones de personas.
Actualmente se están realizando docenas de investigaciones para encontrar el tratamiento o la terapia contra el SARS-CoV-2 que funcione y sea seguro.
Las estrategias incluyen la detección de la mejor manera de neutralizar las proteínas de la espiga del SARS-CoV-2 que hacen que se unan fácilmente a las células humanas en los pulmones y los intestinos, o activar los anticuerpos que hicieron el mejor trabajo al unirse a las proteínas de la espiga del SARS-CoV -2, o ambos.
Los EAU también lideran una terapia pionera basada en células madre para ayudar a curar a los pacientes con COVID-19 .
A diferencia de la ruta de la vacuna, la revolucionaria terapia basada en células madre desarrollada por un equipo de EAU actúa reparando el daño pulmonar a través de un inhalador procedente de células madre activadas extraídas de los propios pacientes.
La licencia estadounidense de Remdesivir, administrada por vía intravenosa, se encuentra bajo el caso de "uso de emergencia" en pacientes con coronavirus.
TRATAMIENTO BASADO EN ANTICUERPOS MONOCLONALES.
Los llamados anticuerpos monoclonales se han convertido en un pilar de la medicina moderna. Ahora se usa para defenderse de una variedad de enfermedades, desde cáncer hasta lupus.
Sin embargo, el desarrollo de tales medicamentos es un proceso notoriamente lento, ya que lleva muchos años de arduo trabajo de ingeniería inversa.
Por ejemplo, Zmapp se desarrolló infectando ratones con Ébola y luego recolectando los anticuerpos que los ratones produjeron contra el virus. El, esos anticuerpos tuvieron que ser diseñados para parecerse más a un anticuerpo humano, para no provocar una reacción inmune.
Los ensayos también toman muchos meses, si no años, para confirmar si el tratamiento es seguro y efectivo.